自从去年开始简化进口药品上市审批流程,中国的消费者开始可以赶在美国、欧洲之前获得一些突破性的药物。全球的药企们也争相布局,准备在中国率先试验和推出特色新药。

(图源:Hindustan Times)
英国的阿斯利康公司(AstraZeneca)将在上海和北京的药店推出其最新的贫血疗法,上市时间大约比在美国市场要早一年。美国巨头礼来公司(Eli Lilly&Co)也与中国合作伙伴共同制定了一套肠癌治疗方法,情况类似。
Polar Capital LLP驻伦敦的医疗保健基金经理丹尼尔·马霍尼(Daniel Mahony)表示,“从现在起20年后,中国的市场规模将与美国相当,甚至可能更大。”“今天在中国获得首次批准可能听起来还很不寻常,但五年后很可能你就不会这么想了。”
在对癌症、糖尿病和肾脏疾病等严重疾病的创新治疗方法“饥渴”了数十年之后,中国的14亿人口正成为全球制药公司的主要目标。他们获得的医疗保险比以往任何时候都多,而且数百万人还会那些不在医保范围内的西药治疗掏腰包。
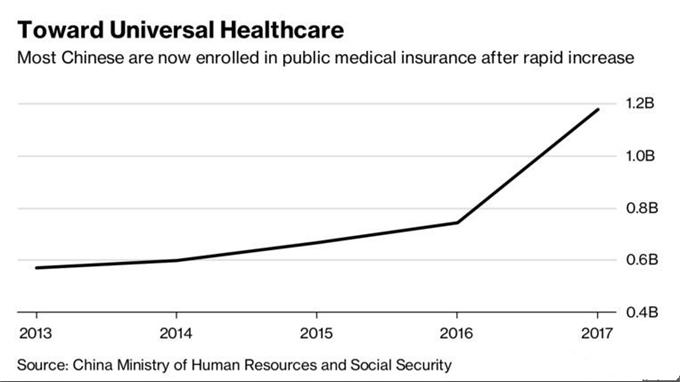
(图源:Bloomberg)
今年5月,国内取消了28种进口药品的关税,并延长了专利保护。
此前,中国繁琐的药品审批程序阻止了许多国外的处方药进入市场。据中国食品药品监督管理局(CFDA)统计,2001年至2016年间,发达国家批准的433种新药处方中,只有不到三分之一到达中国。
去年10月,监管机构废除了一项规定,该规定要求公司在产品获批前在中国重新进行所有药物试验。这一举措是更广泛的改革的一部分,它改变了游戏规则,因为这意味着大型制药公司可能会同时在中国和美国同时推出新药,甚至更快更优先。
越来越多人从关心温饱变成了更关心“如果我得了癌症,会发生什么事?”
AxZeneca正在与旧金山的FibroGen合作,就开发的贫血症药物Roxadustat进行新系统的检测。药监局对其进行了优先审查,并不断更新和进行评估。研究人员完成每项试验后,会将结果公布出来。到2019年上半年,这批药物已经在中国完成所有试验,随后才会在美国FDA申请获批。
“这是一个重要的里程碑,”总部位于英国剑桥的阿斯利康(AstraZeneca)肾脏、心脏和糖尿病部门负责人Ludovic Helfgott表示,该部门预计该监管机构将在年底前获得批准。“这将是第一次在中国首次授权一个全球品牌、全球产品、全球医药。”
虽然在西方获得批准可能仍然更快,但中国赶超的压力却在加剧。在饮食、污染和繁重工作量的变化导致肥胖、糖尿病和哮喘和肠道疾病等炎症状况的普遍存在后,其人口迅速老龄化并且医疗需求显着未得到满足。
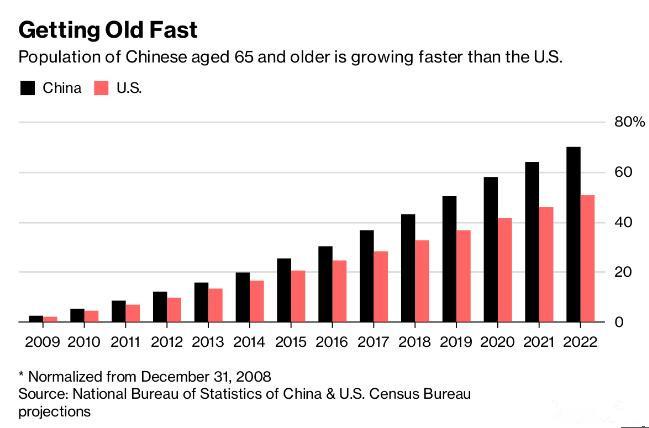
(图源:Bloomberg)
消费者,特别是在激动人心的中产阶级,正在自行解决问题,上个月的“疫苗门”抗议中已经出现了这样的倾向。许多人还选择出国旅游时,甚至在陷入债务时,为家人购买药品。《自然》(Nature)最近的一份报告称,过去五年全球批准的42种抗癌药物中,只有四种在中国销售。
Hogan Lovells LLP律所的律师Xin Tao指出,上个月在国内上映的《我不是药神》更是将中国消费者对药品问题的关注推向临界点。
Eli Lilly正在与和记中国医疗科技(Hutchison China MediTech Ltd. of Hong Kong)合作,准备在获得中国批准后,在今年晚些时候推出用于治疗结肠直肠癌的fruquintinib,随后这一药品会由和记中国医疗科技推向美国和欧洲市场。据WHO数据,全球有近五分之一的结肠直肠癌患者在中国。
为了提高覆盖率,去年公共保险政策增加了100多种西药,包括阿斯利康的心脏病药物Brilinta,以及罗氏控股的Herceptin和葛兰素史克的Viread等癌症治疗药物,其成本比美国或欧洲低50%。“我们没有预测到能在中国市场实现如此迅速的扩张,”FibroGen中国业务副总裁Chris Chung说。
贫血是一种红细胞缺乏症,如果不治疗就会损害器官。而在中国,由于慢性肾病的一种副作用,这种疾病已经引起数千万人的困扰。Roxadustat诱使身体认为氧气水平较低,引发缺氧诱导因子(HIF)的增加,从而增加红细胞和血红蛋白的水平。它将在FibroGen工厂本地生产,作为本十年扩大其本地业务的一部分。
由于加快审批速度的重要性,中国药监局计划在年底前将员工人数增加到1,000人,而2014年该机构的人数还不到100人。
健康数据公司Iqvia Holdings的研究人员预测,到2021年,中国的药品市场将增长30%,达到1700亿美元,大型制药公司当然不会浪费时间和机会。以其糖尿病治疗Actos而闻名的日本制药商武田制药(Takeda Pharmaceutical)计划在未来五年内在中国推出7个产品,比其他任何地方都要多。
“我们在中期的目标是将还在早期发展阶段的中国纳入进来。”武田首席执行官Christophe Weber表示。



















